“램시마SC, 인플릭시맙 정맥주사 제형의 모든 성인 적응증 획득한 최초의 피하주사 제형 될 것”
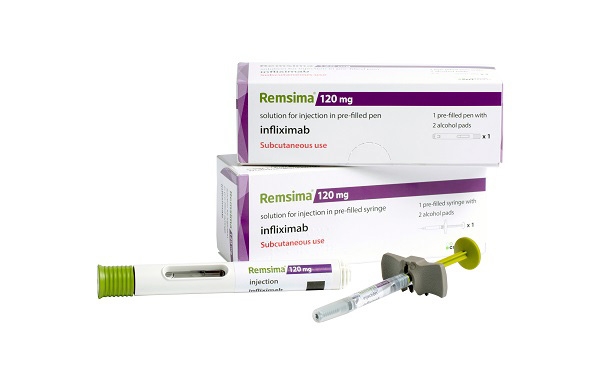
[그린포스트코리아 이민선 기자] 램시마(성분명 인플릭시맙)를 세계 최초로 자가 주사할 수 있는 피하주사 제형으로 개선한 ‘램시마SC’가 유럽에서 염증성 장질환 추가 승인을 권고받으며 17조 시장 공략에 나선다.
셀트리온은 유럽의약품청(EMA) 산하 약물사용자문위원회(CHAP)에서 ‘램시마SC’를 염증성 장질환 등에도 사용할 수 있게 적응증 추가 승인 권고 의견을 받았다고 29일 밝혔다.
셀트리온은 CHMP의 허가 권고는 사실상 유럽 의약품 승인을 의미하는 것으로 보고 있다. CHMP 허가 승인 권고 후 1∼3개월 이내에 유럽연합 집행위원회(EC, European Commission)가 최종 승인하기 때문이다. 램시마SC는 조만간 EC로부터 최종 승인을 획득한 후 유럽 31개 국가에서 판매될 전망이다.
앞서 램시마SC는 지난해 11월 류마티스 관절염 치료 효과로 EMA 허가를 받았다. 지난 25일(현지시간)에는 크론병, 궤양성 대장염 등 염증성 장 질환과 강직성 척추염, 건선성 관절염 및 건선 치료 효과로 추가 승인을 권고받았다.
회사 관계자는 “램시마SC는 유럽연합의 최종 승인을 받으면 유럽 31개국에서 완성형 인플릭시맙 피하주사 제형으로 판매된다”며 “램시마SC는 인플릭시맙 정맥주사 제형의 모든 성인 적응증을 획득한 최초의 피하주사 제형이 될 것”이라고 말했다.
minseonlee@greenpost.kr
이민선 기자
minseonlee@greenpost.kr